La caquèxia és una malaltia sistèmica caracteritzada per pèrdua de pes, atròfia muscular i del teixit adipós i inflamació sistèmica. La caquèxia és una de les principals complicacions i causes de mort en pacients amb càncer. A més del càncer, la caquèxia pot ser causada per diverses malalties cròniques no malignes, com ara la insuficiència cardíaca, la insuficiència renal, la malaltia pulmonar obstructiva crònica, les malalties neurològiques, la sida i l'artritis reumatoide. S'estima que la incidència de caquèxia en pacients amb càncer pot arribar al 25% al 70%, cosa que afecta greument la qualitat de vida (QdV) dels pacients i agreuja la toxicitat relacionada amb el tractament.
La intervenció eficaç de la caquèxia és de gran importància per millorar la qualitat de vida i el pronòstic dels pacients amb càncer. No obstant això, malgrat alguns avenços en l'estudi dels mecanismes fisiopatològics de la caquèxia, molts fàrmacs desenvolupats basats en possibles mecanismes només són parcialment eficaços o ineficaços. Actualment no hi ha cap tractament eficaç aprovat per la Food and Drug Administration (FDA) dels Estats Units.
Hi ha moltes raons per al fracàs dels assajos clínics sobre la caquèxia, i la raó fonamental pot raure en la manca d'una comprensió completa del mecanisme i el curs natural de la caquèxia. Recentment, el professor Xiao Ruiping i l'investigador Hu Xinli de la Facultat de Tecnologia del Futur de la Universitat de Pequín han publicat conjuntament un article a Nature Metabolism, que revela el paper important de la via làctic-GPR81 en l'aparició de la caquèxia cancerosa, proporcionant una nova idea per al tractament de la caquèxia. Resumim això sintetitzant articles de Nat Metab, Science, Nat Rev Clin Oncol i altres revistes.
La pèrdua de pes sol ser causada per una reducció de la ingesta d'aliments i/o un augment de la despesa energètica. Estudis previs han suggerit que aquests canvis fisiològics en la caquèxia associada a tumors són impulsats per certes citocines secretades pel microambient tumoral. Per exemple, factors com el factor de diferenciació del creixement 15 (GDF15), la lipocalina-2 i la proteïna similar a la insulina 3 (INSL3) poden inhibir la ingesta d'aliments unint-se a llocs reguladors de la gana al sistema nerviós central, provocant anorèxia en els pacients. La IL-6, la PTHrP, l'activina A i altres factors impulsen la pèrdua de pes i l'atròfia tissular activant la via catabòlica i augmentant la despesa energètica. Actualment, la investigació sobre el mecanisme de la caquèxia s'ha centrat principalment en aquestes proteïnes secretades, i pocs estudis han implicat l'associació entre els metabòlits tumorals i la caquèxia. El professor Xiao Ruiping i l'investigador Hu Xinli han adoptat un nou enfocament per revelar l'important mecanisme de la caquèxia relacionada amb tumors des de la perspectiva dels metabòlits tumorals.
Primer, l'equip del professor Xiao Ruiping va analitzar milers de metabòlits a la sang de controls sans i ratolins models de caquèxia de càncer de pulmó, i va descobrir que l'àcid làctic era el metabòlit més significativament elevat en ratolins amb caquèxia. El nivell sèric d'àcid làctic va augmentar amb el creixement del tumor i va mostrar una forta correlació amb el canvi de pes dels ratolins amb tumors. Les mostres sèriques recollides de pacients amb càncer de pulmó confirmen que l'àcid làctic també juga un paper clau en la progressió de la caquèxia del càncer humà.
Per determinar si els nivells alts d'àcid làctic causen caquèxia, l'equip de recerca va administrar àcid làctic a la sang de ratolins sans a través d'una bomba osmòtica implantada sota la pell, elevant artificialment els nivells sèrics d'àcid làctic fins al nivell dels ratolins amb caquèxia. Després de 2 setmanes, els ratolins van desenvolupar un fenotip típic de caquèxia, com ara pèrdua de pes, atròfia del teixit adipós i muscular. Aquests resultats suggereixen que la remodelació del greix induïda pel lactat és similar a la induïda per les cèl·lules canceroses. El lactat no és només un metabòlit característic de la caquèxia cancerosa, sinó també un mediador clau del fenotip hipercatabòlic induït pel càncer.
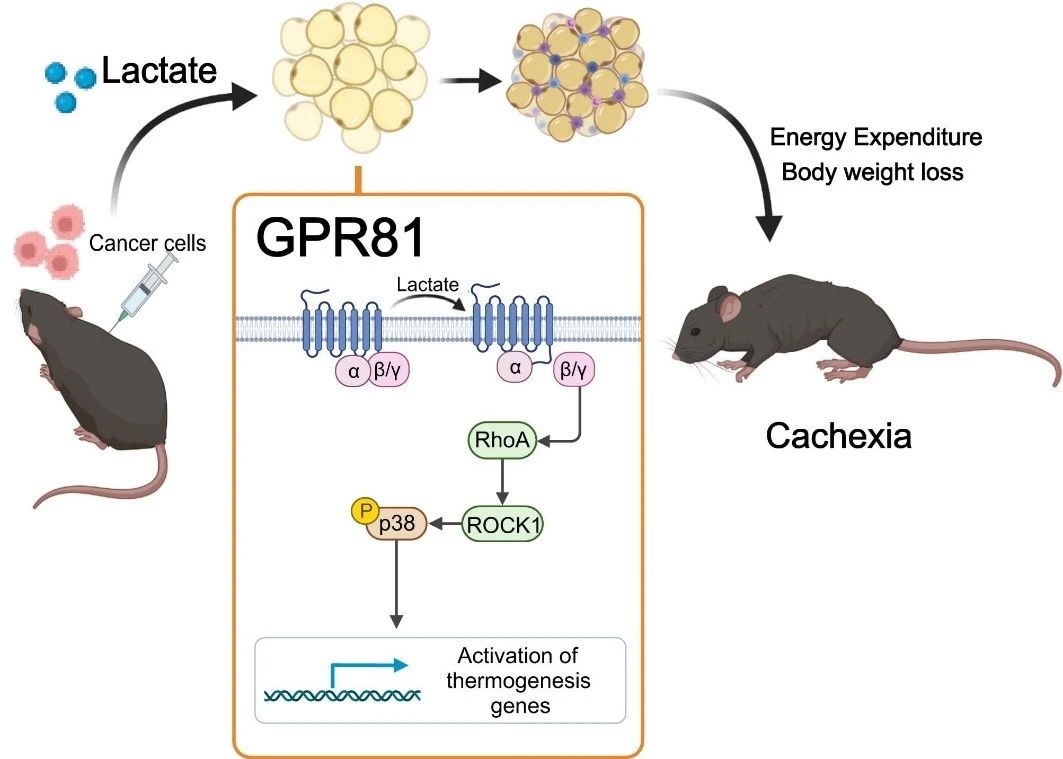
A continuació, van descobrir que la deleció del receptor de lactat GPR81 era eficaç per alleujar les manifestacions de caquèxia induïda per tumors i lactat sèric sense afectar els nivells de lactat sèric. Com que el GPR81 s'expressa molt en el teixit adipós i els canvis en el teixit adipós abans que en el múscul esquelètic durant el desenvolupament de la caquèxia, l'efecte knockout específic del GPR81 en el teixit adipós del ratolí és similar al de la knockout sistèmica, millorant la pèrdua de pes induïda per tumors i el consum de greix i múscul esquelètic. Això suggereix que el GPR81 en el teixit adipós és necessari per al desenvolupament de la caquèxia cancerosa impulsada per l'àcid làctic.
Estudis posteriors van confirmar que després d'unir-se a GPR81, les molècules d'àcid làctic impulsen l'enfosquiment dels greixos, la lipòlisi i l'augment de la producció de calor sistèmica a través de la via de senyalització Gβγ-RhoA/ROCK1-p38, en lloc de la via clàssica PKA.
Malgrat els resultats prometedors en la patogènesi de la caquèxia relacionada amb el càncer, aquestes troballes encara no s'han traduït en tractaments eficaços, per la qual cosa actualment no hi ha estàndards de tractament per a aquests pacients, però algunes societats, com l'ESMO i la Societat Europea de Nutrició Clínica i Metabolisme, han desenvolupat guies clíniques. Actualment, les guies internacionals recomanen fermament promoure el metabolisme i reduir el catabolisme mitjançant enfocaments com la nutrició, l'exercici i la medicació.
Data de publicació: 28 d'abril de 2024