La hiperlipidèmia mixta es caracteritza per nivells plasmàtics elevats de lipoproteïnes de baixa densitat (LDL) i lipoproteïnes riques en triglicèrids, cosa que augmenta el risc de patir malaltia cardiovascular ateroscleròtica en aquesta població de pacients.
L'ANGPTL3 inhibeix la lipoproteïna lipasa i l'endosèpiasa, així com l'absorció hepàtica de lipoproteïnes riques en triglicèrids. Els portadors de la variant inactivada d'ANGPTL3 tenien nivells més baixos de triglicèrids, colesterol LDL, colesterol de lipoproteïnes d'alta densitat (HDL) i colesterol no HDL, així com un menor risc de malaltia cardiovascular ateroscleròtica. El zodasiran és un fàrmac amb un petit ARN interferent (ARNi) que té com a objectiu l'expressió d'ANGPTL3 al fetge.
La hiperlipidèmia mixta es refereix a nivells elevats de colesterol lipoproteic de baixa densitat (LDL-C) i lipoproteïnes riques en triglicèrids. Les lipoproteïnes riques en triglicèrids (inclosos els quilomicrons, les lipoproteïnes de molt baixa densitat (VLDL) i el colesterol residual) tenen un paper important en el desenvolupament de la malaltia ateroscleròtica. No hi ha cap tractament eficaç per a la hiperlipidèmia mixta.
Se sap que els fàrmacs Bates redueixen els nivells de triglicèrids (TG), però la reducció és limitada. Alhora, els fàrmacs que redueixen els TG, inclosos els fàrmacs Bates (com l'àcid acètic eicosapentaenoic, etc.), no tenen cap efecte significatiu sobre el risc de malaltia ateroscleròtica causada per nivells elevats de colesterol residual. A més, estudis previs en pacients que ja prenen estatines han demostrat que la combinació de fàrmacs que redueixen els TG no redueix el risc d'esdeveniments cardiovasculars. Aquests factors dificulten molt el tractament de la hiperlipidèmia mixta.
L'ANGPTL3 (proteïna similar a l'angiopoietina 3) regula el metabolisme dels lípids i les lipoproteïnes, incloent-hi els TG i el colesterol que no és de lipoproteïnes d'alta densitat (HDL-C), mitjançant la inhibició reversible de la captació de lipoproteïnes hepàtiques dependent del receptor de la lipoproteïna lipasa, l'endosèpiasa i la lipoproteïna de baixa densitat (LDL). S'ha descobert que la variant d'inactivació de l'ANGPTL3 condueix a un augment de l'activitat de la lipoproteïna lipasa i l'endosèpiasa, que al seu torn condueix a nivells baixos de lipoproteïnes plasmàtiques en la majoria dels casos. Aquests inclouen lipoproteïnes riques en triglicèrids (és a dir, quilomicrons, colesterol residual, VLDL, lipoproteïnes de densitat mitjana [IDL]), LDL, lipoproteïnes d'alta densitat (HDL), lipoproteïna (a) i els seus components de colesterol. Les persones heterozigotes que porten aquesta variant tenen un risc reduït d'aproximadament un 40% de patir malaltia ateroscleròtica, i no s'ha trobat cap fenotip clínic advers. L'ANGPTL3 s'expressa al fetge, i les teràpies de silenciament gènic dirigides al seu ARNm, conegudes com a fàrmacs de petits ARN interferents (siRNA), són un tractament híbrid prometedor per a la hiperlipidèmia.
El 12 de setembre de 2024, el New England Journal of Medicine (NEJM) va publicar un estudi ARCHES 2 que confirmava que el fàrmac de siRNA zodasiran reduïa significativament els nivells de TG en pacients amb hiperlipidèmia mixta [1]. ARCHES-2 és un assaig de fase 2b d'exploració de rang de dosi, doble cec i controlat amb placebo. Es van inscriure un total de 204 pacients amb hiperlipidèmia mixta (nivells de TG en dejú de 150-499 mg/dL, nivells de LDL-C ≥70 mg/dL o nivells de no HDL-C ≥100 mg/dL). Es van dividir en grup de zodasiran 50 mg, grup de 100 mg, grup de 200 mg i grup de control amb placebo. Els pacients van rebre injeccions subcutànies a la setmana 1 i 12, i van rebre profilaxi de seguiment fins a la setmana 36.
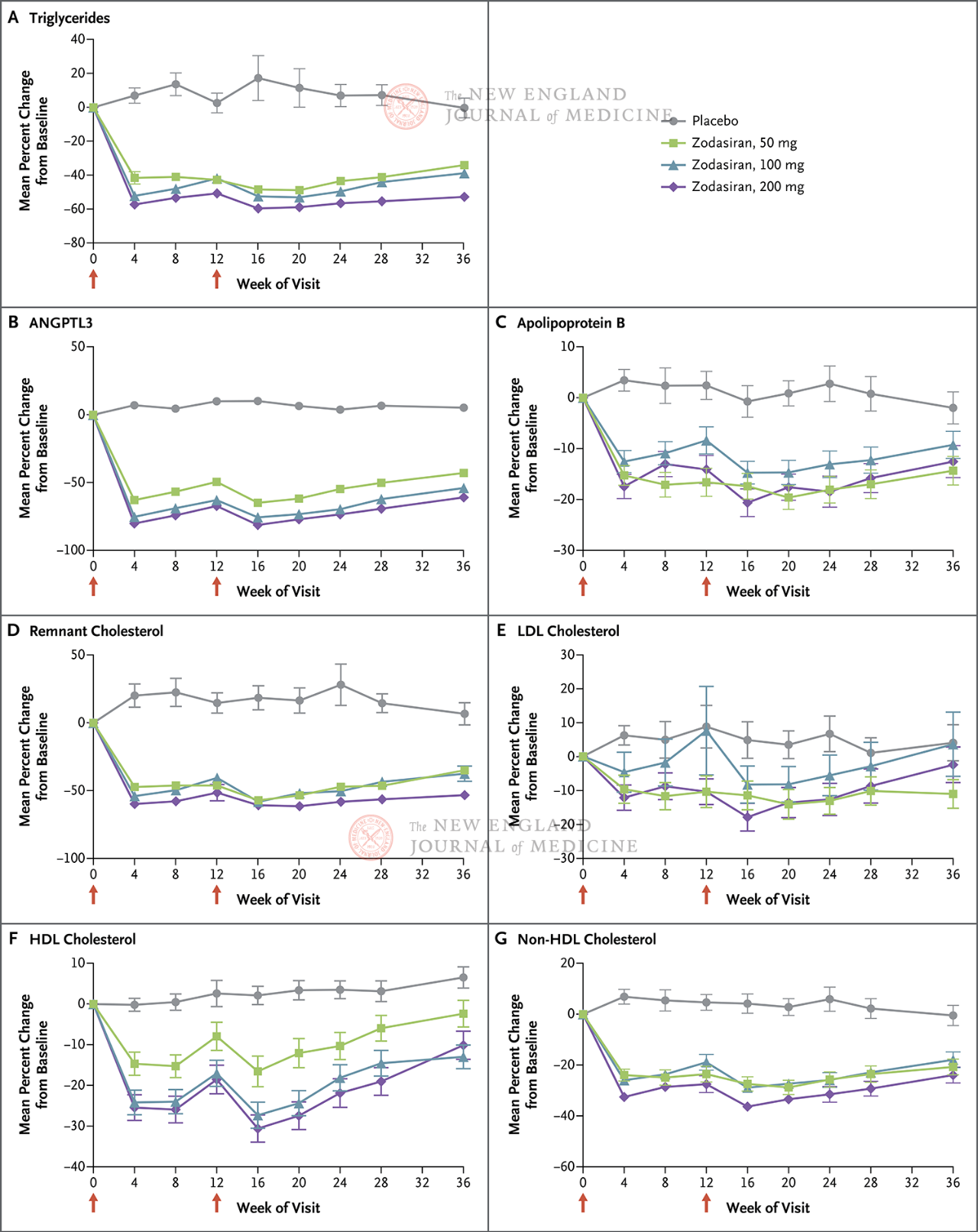
El criteri d'avaluació principal va ser el canvi percentual en els TG des del punt de partida fins a la setmana 24. L'estudi va trobar que, a la setmana 24, els nivells de TG en el grup de zodasiran es van reduir significativament de manera dependent de la dosi (els nivells de TG en cada grup de dosi es van reduir en 51, 57 i 63 punts percentuals, respectivament, en comparació amb els del grup placebo) (P <0,001 per a totes les comparacions). L'ANGPTL3 també va disminuir en 54 punts percentuals, 70 punts percentuals i 74 punts percentuals, respectivament. Els nivells de no HDL-C van disminuir en 29 punts percentuals, 29 punts percentuals i 36 punts percentuals, els nivells d'apolipoproteïna B van disminuir en 19 punts percentuals, 15 punts percentuals i 22 punts percentuals, i els nivells de LDL-C van disminuir en 16 punts percentuals, 14 punts percentuals i 20 punts percentuals, respectivament, i aquests resultats van persistir fins a la setmana 36. A la setmana 24, el zodasiran
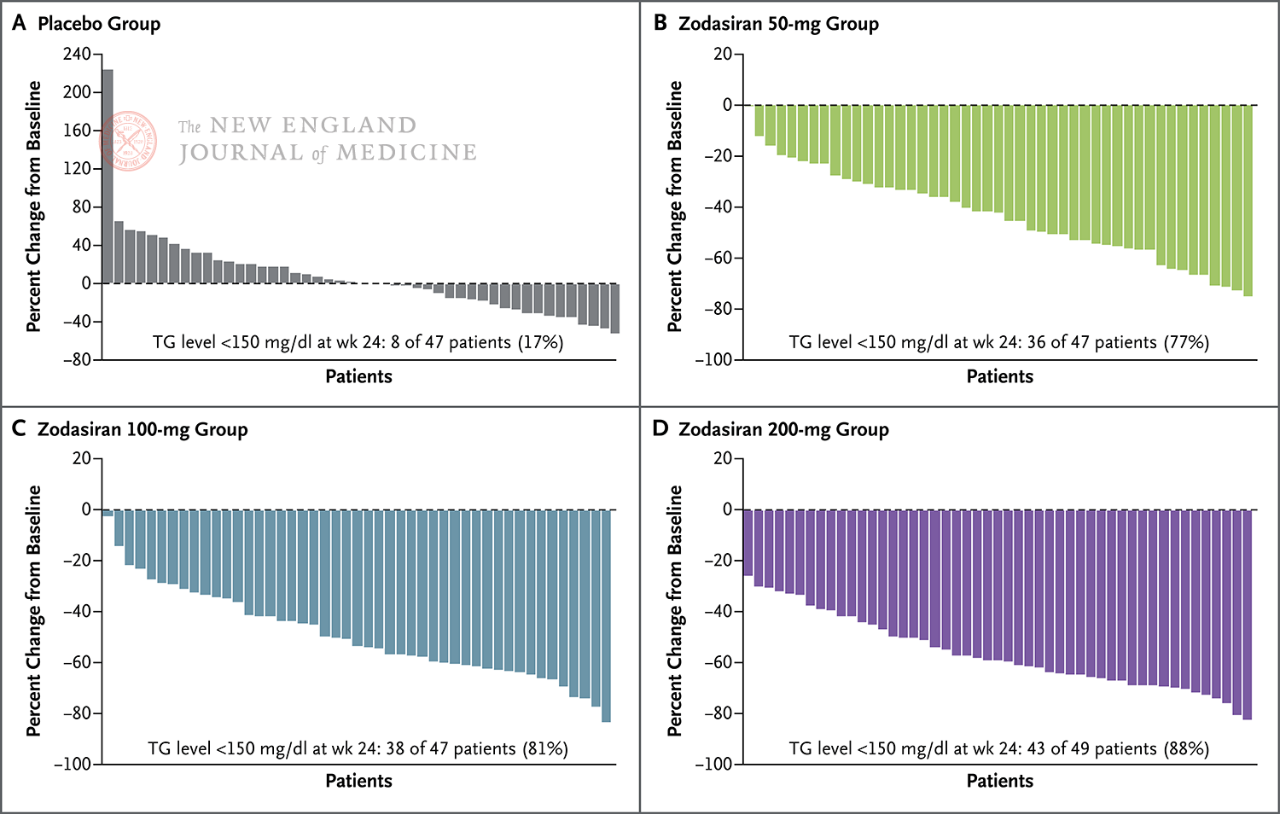
En el 88% dels pacients del grup de 200 mg, els TG en dejú havien caigut al rang normal.
Les fletxes vermelles dels dies 1 i 12 indiquen l'administració de zodasiran o placebo.
Els nivells de TG en dejú van disminuir a la normalitat a la setmana 24 (150
mg/dL o menys)
Cada pilar representa un pacient.
L'estudi també va observar que el *zotasiran* era segur en tots els grups de dosi, amb només 2 pacients que van interrompre l'estudi a causa d'esdeveniments adversos (1 al grup placebo i 1 al grup de *zotasiran* de 100 mg). Tots els esdeveniments adversos greus del grup de *zotasiran* es van recuperar al final de l'estudi, i hi va haver una mort al grup placebo. L'únic esdeveniment advers preocupant va ser un augment de l'HBA1c en el grup de *zotasiran* de 200 mg en comparació amb el placebo (canvi mitjà des del començament fins a la setmana 24 [± DE], 0,38±0,66% vs. -0,03±0,88% en pacients amb diabetis preexistent). Els pacients sense diabetis eren del 0,12±0,19% vs. -0,03±0,19%).
En particular, gairebé tots els pacients de l'estudi (96%) estaven sent tractats amb estatines (el 37% dels quals eren estatines en dosis altes), l'1% estaven sent tractats amb un inhibidor de la subtilisina 9 de l'enzim convertidor de proproteïnes (PCSK9i) i el 21% estaven sent tractats amb fibrats. Per tant, l'addició de zodasiran sobre la base del règim de tractament convencional actual encara aconseguia efectes considerables de reducció dels lípids, cosa que proporciona un nou règim per al tractament de la hiperlipidèmia mixta en el futur.
A la setmana 24, la dosi màxima de 200 mg de *zotasiran* a l'estudi va reduir els nivells de colesterol residual en 34,4 mg/dL en comparació amb el placebo. Segons els models actuals, s'espera que aquesta reducció redueixi els principals esdeveniments adversos cardíacs en un 20%. *zodasiran* té el potencial de ser utilitzat com a monoteràpia per a tots els components lipoproteics per reduir el risc d'esdeveniments cardiovasculars en pacients. Per tant, cal més investigació per determinar el potencial d'aquest fàrmac per reduir el risc de malaltia ateroscleròtica.
L'estudi MUIR de fase 2b, doble cec, aleatoritzat i controlat amb placebo, publicat simultàniament a NEJM, va utilitzar un altre fàrmac de siRNA, el plozasiran, per tractar la hiperlipidèmia mixta [2]. El plozasiran està dissenyat per reduir l'expressió d'APOC3, el gen que codifica l'apolipoproteïna C3 (APOC3), un regulador del metabolisme dels TG, al fetge, reduint així els nivells de TG i de colesterol residual. Les reduccions dels nivells de TG i colesterol residual observades a l'estudi van ser similars a les trobades a l'estudi ARCHES-2. Per tant, s'especula que en pacients amb hiperlipidèmia mixta, els dos fàrmacs tenen efectes similars en la reducció del nivell de lipoproteïnes riques en triglicèrids i del colesterol residual.
Els resultats dels dos estudis de siRNA mostren que es tracta d'una classe de fàrmacs molt prometedora que aportarà noves opcions per al tractament de la hiperlipidèmia mixta i millorarà els resultats cardiovasculars en els pacients.
Data de publicació: 15 de setembre de 2024